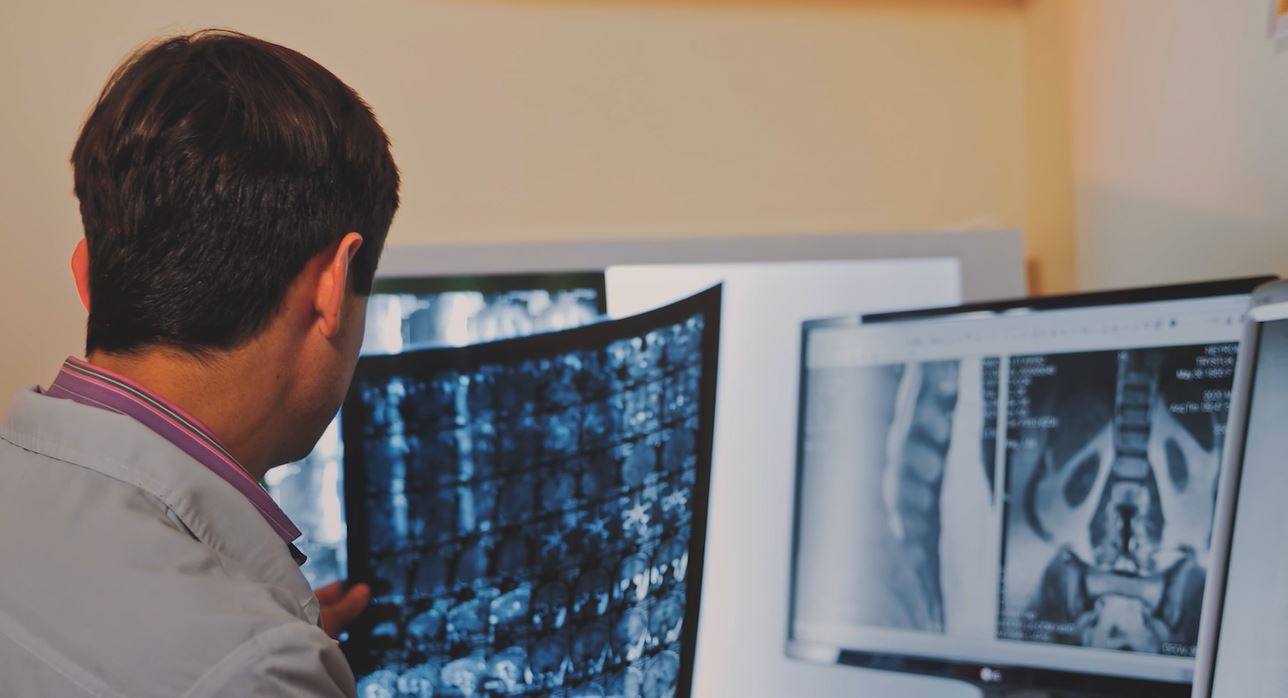
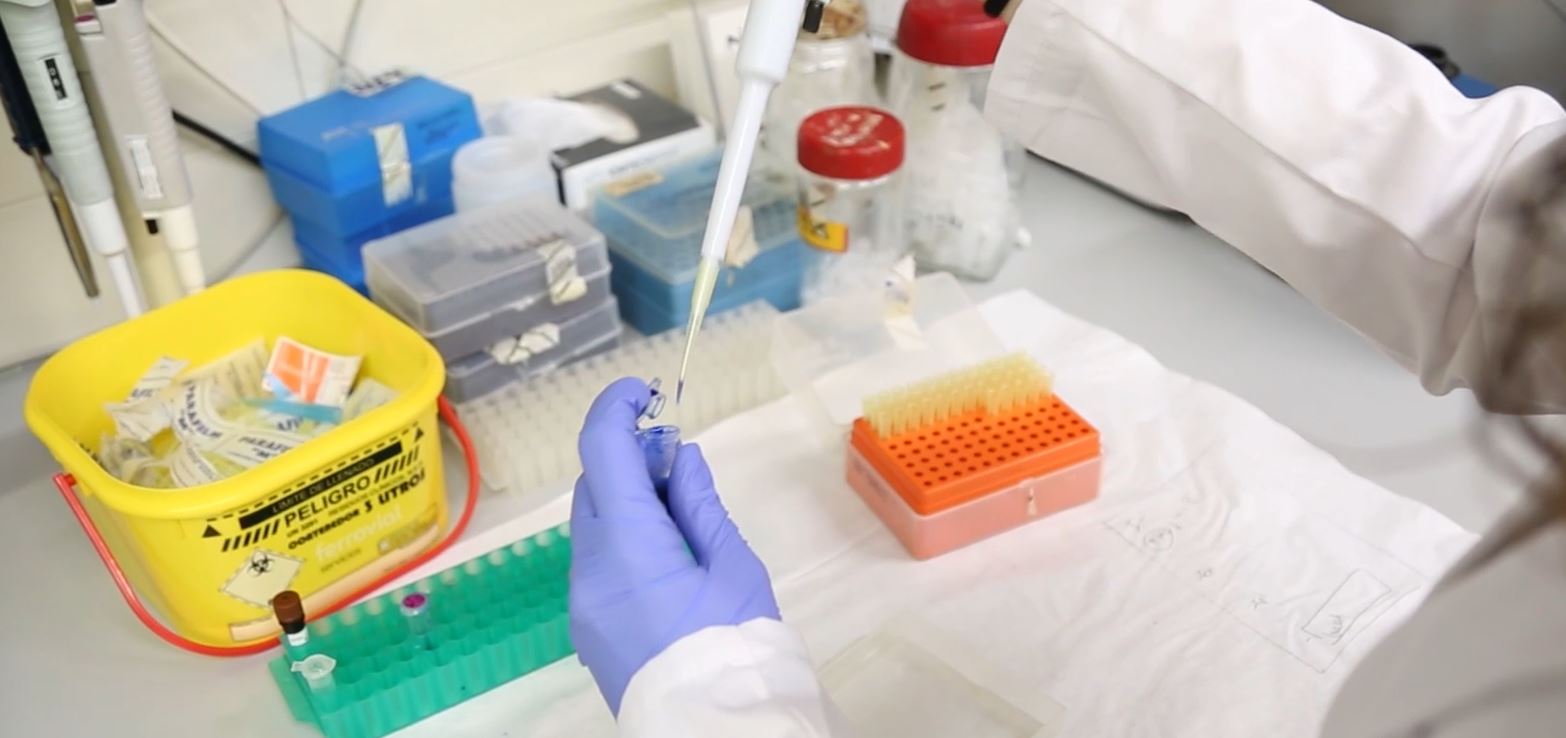
Coordinador/a d'assajos clínics
Altres denominacions
Investigador/a principal
Descripció
La Llei del Medicament defineix l'assaig clínic com "tota avaluació experimental d'una substància o medicament, a través de la seva administració o aplicació a éssers humans". El procés d'aprovació d'un nou medicament per a l'ús humà és complex i de llarga durada. Després de la recerca preclínica (in vitro i amb animals), un nou medicament es prova amb humans durant els assajos clínics (fase II, fase III i fase IV, segons el tipus de poblacions i nombre de pacients inclosos). Normalment, tot el procés implica almenys 3.000 persones, dura entre cinc i deu anys i pot tenir un cost total d'entre 300 i 500 milions d'euros. Per aprovar-lo, cal presentar tota la documentació científica dels protocols seguits i els resultats obtinguts.
El/la coordinador/a d'assajos clínics és responsable dels assajos clínics d'una empresa (bio)farmacèutica o CRO (contract research organization) de recerca clínica. Generalment, es tracta d'un/a professional que dirigeix un equip de vàries persones especialistes en àmbits diferents (assistents, monitors/res d'assajos clínics, bioestadístics/ques i informàtics/ques).Col·labora estretament amb les autoritats, els/les metges especialistes o líders d'opinió i els departaments interns d'R+D.
Tasques
- En estreta col·laboració amb la direcció mèdica, defineix l'estratègia de recerca clínica d'acord amb les prioritats estratègiques de l'empresa.
- Al seu càrrec estan l'estratègia, el plantejament i el desenvolupament de les activitats clíniques per a l'aprovació d'un nou fàrmac.
- Estableix l'estratègia i dirigeix el pla clínic de cada producte.
- Defineix les relacions amb les CROs, supervisa els protocols dels assajos clínics, la identificació dels/de les investigadors/es principals i participa als grups de treball.
- Determina els requisits operacionals i materials dels estudis.
- Determina els pressupostos i mecanismes de finançament necessaris dels estudis.
- Treballa seguint la normativa regulatòria requerida (EMA, FDA) per a cada tipus de productes i patologia.
- Treballa sota els estàndards de qualitat de Bones Pràctiques Clíniques (GCP - Good Clinical Practices) i la responsabilitat corporativa de l'empresa.
- Garanteix que s'informi sobre el nou medicament als/a les pacients que participen a l'estudi.
- Redacta informes científics sobre les conclusions d'eficàcia i seguretat dels fàrmacs i presenta resultats a revistes i congressos.
- Defineix i coordina la formació dels membres del seu equip: assistents, monitors/res d'assajos clínics (CRA), bioestadístics/ques i informàtics/ques.
- Divulga els darrers informes clínics als líders d'opinió, responsables acadèmics/ques, experts/es, científics/ques, col·lectiu mèdic.










 | català | principiant
| català | principiant | català | avançat
| català | avançat
 Obrir
Obrir | català | principiant
| català | principiant